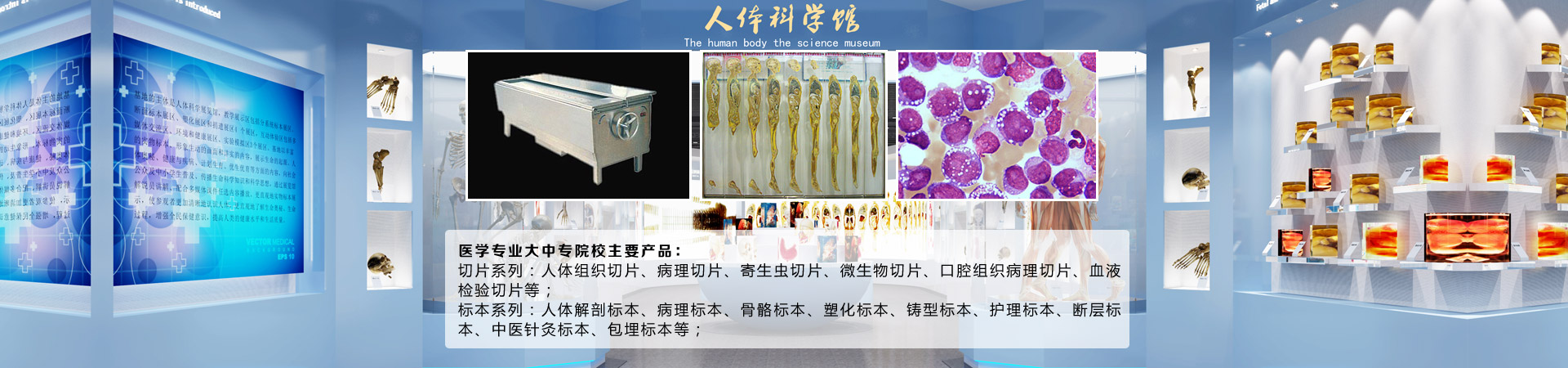
各种组织切片方法的操作和优缺点分析
组织切片伴随着显微镜技术和免疫实验等的发展而得到广泛的应用。本文对其中的冰冻切片、石蜡切片、碳蜡切片、超薄切片、塑料切片等几种常用的实验方法相关操作步骤进行介绍。
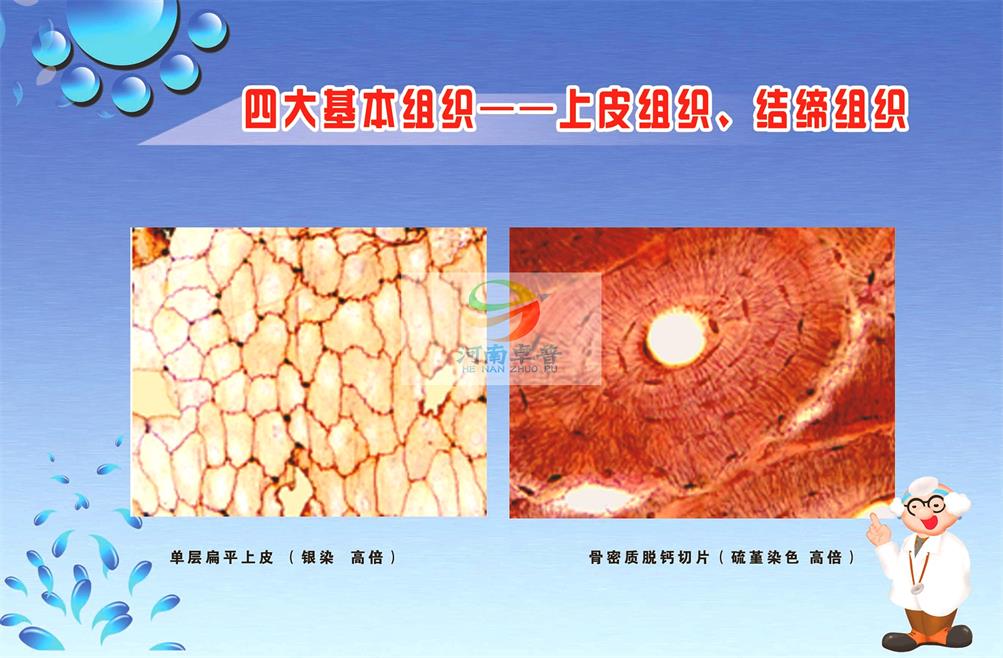
冰冻切片
是免疫组织化学染色中最常用的一种切片方法。其最突出的优点是能够较完好地保存多种抗原的免疫活性,尤其是细胞表面抗原更应 采用冰冻切片。新鲜的组织及已固定的组织均可作冰冻切片。
冰冻时,组织中水份易形成冰晶,往往影响抗原定位。一般认为冰晶少而大时,影响较小,冰晶小而多时,对组织结构损害较大,在含水量较多的组织中上述现象更易发生。冰晶的大小与其生长速率成正比,而与成核率(形成速率)成反比,即冰晶形成的数量愈多则愈小,对组织结构影响愈严重。因此,应尽量降低冰晶的数量。Fish认为冰冻开始时,冰晶成核率较慢,以后逐渐增加,其临界温度为-33。C, 从-30。C降至-43。C之间,成核率急剧增加达1018,然后再减慢。基于上述理论可采取以下措施减少冰晶的形成。
(1)速冻,使组织温度骤降,缩短从-33。C43。C的时间,减少冰晶的形成。其方法有二:
①干冰-丙酮(酒精)法:将150-200ml丙酮(酒精)装入小保温杯内,逐渐加入干冰,直至饱和呈粘稠状,再加干冰不再昌泡时,温度可达-70℃C,用一小烧杯(50-100ml)内装异戊烷约50ml,再将烧杯缓慢置入干冰丙酮(纯酒精)饱和液内,至异戊烷温度达-70℃时即可使用。将组织(大小为1cm×0.8cm×0.5cm)投入异戊烷内速冻30-60s后取出,或置恒冷箱内以备切片,或置-80℃低温冰箱内贮存。
②液氮法:将组织块平放于软塑瓶盖或特制小盒内(直径约2cm),如组织块小可适量加OCT包埋剂浸没组织,然后将特制小盒缓缓平放入盛有液氮的小杯内,当盒底部接触液氮时 即开始气化沸腾,此时小盒保持原位切勿浸入液氮中,大约10-20s组织即迅速冰结成块。取出组织冰块立即置入-80℃冰箱贮存备用,或置入恒冷箱切片机冰冻切片。
(2)将组织置于20%-30%蔗糖溶液1~3天,利用高渗吸收组织中水分,减少组织含水量。
影响冰冻切片的因素较多,因此,技术难度较大,选择好的冰冻切片机是保证切片质量的关键。目前冰冻切片机有两类:
①恒慢冰冻切片机(Cryastat):为较理想的冰冻切片机,型号很多,但其基本结构是将切片机置于-30℃C低温密闭室内,故切片时不受外界温度和环境影响,可连续切薄片至2-4μm,完全能满足免疫组织化学标记要求。切片时,低温室内温度以-15℃~18℃为宜,温度过低组织易破碎,抗卷板的位置及角度要适当,载玻片附贴组织切片,切勿上下移动。
②开放式冰冻切片机:包括半导体致冷切片机和甲醇致冷切片以及老式的CO2、氯乙烷等冷冻切片机。切片时暴露空气中,温度不易控制,切片技术难度 大,在高温季节 ,切片更加困难,且切片厚8~15μm,不易连续切片,但其优点是价廉,国内有生产。
冰冻切片后如不染色,必须吹干,贮存低温冰箱内, 或进行短暂预固定后贮存冰箱保存
石蜡切片
其优点是组织结构保存良好,在病理和回顾性研究中有较大的实用价值,能切连续薄片,组织结构清晰,抗原定位准确。用于免疫组化技术的石蜡切片制备与常规制片略有不同:①脱水、透明等过程应在4℃。C下进行,以尽量减少组织抗原的损失。②组织块大小应限于2cm×1.5cm×0.2cm,使组织充分脱水、透明、浸蜡。③浸蜡、包埋过程中,石蜡应保持在60℃以下,以溶点低的软蜡最好(即低温石蜡包埋)。
以上全过程为18-24h,也可在室温内使用自动脱水机代替。如组织块小,直径小于0.5cm,可用快速石蜡包埋切片,全过程只需4h左右。

石蜡切片为常规制片技术,切片机多为轮转式,切片厚度2~7μm,应用范围广,不影响抗体的穿透性,染色均匀一致。由于甲醛固定、有机熔剂和包埋剂对组抗原有一定的损害及遮蔽,使抗原特征发生改变。有人报告经蛋白酶消化,可以改善光镜免疫组化染色强度,常用的有胰蛋白酶、链霉蛋白酶及胃蛋白酶等消化法。石蜡切片应入37℃恒温箱过夜,这样烤片可减少染色中脱片现象。切片如需长期贮存,可存放于4℃冰箱内备用。
石蜡切片优点较多,但在制片过程中要经过酒精、二甲苯等有机溶剂处理,组织内抗原活性失去较多,有人采用冷冻干燥包埋法(Freeze drying embedding methed),可以保存组织内可溶性物质,防止蛋白变性和酶的失活,从而减少了抗原的丢失。该法是将新鲜组织低温速冻,利用冷冻干燥机(Freezing dryer)在真空、低温条件下排除组织内水分 ,然后用甲醛蒸气固定干燥的组织,最后将组织浸蜡、包埋、切片。此法可用于免疫荧光标记、免疫酶标记及放射自显影。
振动切片
用振动切片机(Vibratotme),可以把新鲜组织(不固定不冰冻)切成厚片20~100μm,以漂浮法在反应板进行免疫组织化学染色,然后在解剖显微镜下检出免疫反应阳性部位,修整组织进行后固定,最后按电镜样品制备、脱水、包埋、超薄切片、染色观察等。组织不冰冻,无冰晶形成和组织抗原破坏,在免疫组化染色前避免了组织脱水、透明、包埋等步骤对抗原的损害,能较好地保留组织内脂溶性物质和细胞膜抗原,主要用于显示神经系统抗原分布研究。这种包埋前染色,尤其实用于免疫电镜观察。
塑料切片
塑料包埋切片常用包埋剂有甲基丙烯酸盐类(Glycol methacrylate, GMA)及环氧树脂类(Epon 812,618),其优点是可以同时作光镜和电镜检测,能相互对照所查抗原,定位准确。塑料包埋切片可切出比石蜡切片更薄的切片,光镜切片可薄至0.5~2um,故称半薄切片(Semithin section)。GMA保存抗原较好,不与组织产生共聚合,但形态学结构欠佳。环氧树脂如Fpon和Araldite能较好地保存形态学结构,但在聚合过程中易和组织起作用,改变抗原结构。塑料包埋切片由于处理程序繁多,抗原活性易丢失。同时半薄切片进行免疫染色时,抗血清不易穿透树脂,因此,塑料切片主要用于免疫电镜的超微切片前定位。包埋前染色的标本,切片薄切片后不需染色,直接在相差显微镜下观察免疫反应部位呈黑点状,定位后进一步作超薄切片,这样,可以明显提高免疫电镜阳性检出率。
超薄切片
电镜标本制作,应用超薄切片机(Ultrotome)进行切片。
碳蜡切片
碳蜡(Carbowax),学名聚乙烯二醇(Polyethlene glycol, PEG)为水溶性蜡。根据其分子量不同,碳蜡有多种,如400、800、1000、1500、4000、6000等,用于组织包埋的有1500、4000两种,其熔点分别38℃C和52。C左右,常温下为固体石蜡状,加温熔化呈液体状。
本法的特点是组织固定水洗后,不需脱水透明可直接浸蜡包埋,且切片方法与常规石蜡切片相同。切下的组织片漂浮水面后自然展开,碳虹迅速深化,组织片即可展平,制片过程简单易行。
具体操作简述如下:组织块不宜过大,一般限定在1.5cm×1cm×0.1cm以内。①组织固定后充分水洗去除固定液,用滤纸吸干组织表面水。②将组织浸入碳蜡(1500)内,45℃30min。③再次浸入混合混合碳蜡液(1500和4000等量混合液),52℃ 30min。④浸入等量混合碳蜡液(或根据气温、湿度变化调整4000和5000混合比例,如气温高湿度大可以4000:1500=3:2混合,反之,则2:3混合)。⑤用等量混合碳蜡或调整混合碳蜡包埋成组织蜡块。⑥切片与石蜡切片相同。在操作过程中,碳蜡组织块应尽量避免与水或冰接触,贮存时应密封干燥冷藏。
本法优点是操作程序减少,时间缩短,组织不经有机溶剂损害、温度低、抗原性保存比石蜡切片好,组织结构清晰。缺点是夏季室温高时切片较困难,连续切片不如石蜡切片顺利;由于碳蜡有强吸湿性,不易长期保存。